Polare und unpolare Dielektrika
Nach Ansicht der klassischen Physik unterscheiden sich Dielektrika grundsätzlich von Leitern, da in ihnen unter normalen Bedingungen keine freien elektrischen Ladungen vorhanden sind. Die Gesamtladung der Teilchen, die dielektrische Moleküle bilden, ist Null. Dies bedeutet jedoch keineswegs, dass die Moleküle dieser Stoffe keine elektrischen Eigenschaften aufweisen können.
Alle bekannten linearen Dielektrika lassen sich in zwei große Gruppen einteilen: polare Dielektrika und unpolare Dielektrika. Diese Unterteilung wird aufgrund der Unterschiede in den Polarisationsmechanismen der Moleküle jeder Art von Dielektrikum eingeführt. Tatsächlich erweist sich der Polarisationsmechanismus als äußerst wichtiger Aspekt bei der Untersuchung sowohl der physikalischen und chemischen Eigenschaften von Dielektrika als auch bei der Untersuchung ihrer elektrischen Eigenschaften.
Unpolare Dielektrika
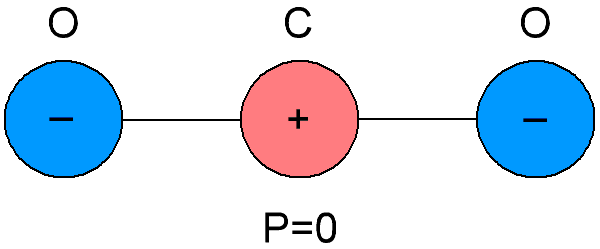
Unpolare Dielektrika werden auch neutrale Dielektrika genannt, da sich die Moleküle, aus denen diese Dielektrika bestehen, durch das Zusammenfallen der Schwerpunkte der negativen und positiven Ladungen in ihrem Inneren unterscheiden.Als Ergebnis stellt sich heraus, dass die Moleküle unpolarer Dielektrika kein eigenes elektrisches Moment haben, es ist gleich Null. Und ohne ein äußeres elektrisches Feld sind die positiven und negativen Ladungen der Moleküle solcher Stoffe symmetrisch angeordnet.
Wenn ein äußeres elektrisches Feld an ein unpolares Dielektrikum angelegt wird, werden die positive und negative Ladung in den Molekülen aus ihrer ursprünglichen Gleichgewichtslage verschoben, die Moleküle werden zu Dipolen, deren elektrische Momente nun proportional zur Stärke des Stroms sind auf sie angewendetes Feld und wird parallel zum Feld ausgerichtet.
Beispiele für unpolare Dielektrika, die heute erfolgreich als elektrische Isoliermaterialien eingesetzt werden, sind: Polyethylen, Polystyrol, Kohlenwasserstoffe, Erdöl-Isolieröle usw. Auch helle Vertreter unpolarer Moleküle sind beispielsweise Stickstoff, Kohlendioxid, Methan usw. Herr.
Unpolare Dielektrika werden aufgrund ihrer niedrigen Tangenswerte für den dielektrischen Verlust häufig als Hochfrequenzdielektrika in Kondensatoren wie dem K78-2 verwendet.
Polare Dielektrika
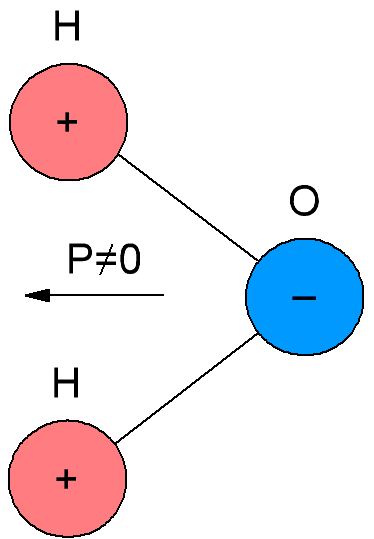
In polaren Dielektrika, die auch Dipoldielektrika genannt werden, haben die Moleküle ein eigenes elektrisches Moment, das heißt, ihre Moleküle sind polar. Der Grund dafür ist, dass die Moleküle polarer Dielektrika eine asymmetrische Struktur haben, sodass die Massenschwerpunkte negativer und positiver Ladungen in den Molekülen solcher Dielektrika nicht zusammenfallen.
Wenn in einem unpolaren Polymer einige der Wasserstoffatome durch Atome anderer Elemente oder durch Nicht-Kohlenwasserstoffradikale ersetzt werden, erhalten wir nur ein polares (Dipol-)Dielektrikum, da dadurch die Symmetrie gebrochen wird Ersatz. Um die Polarität eines Stoffes anhand seiner chemischen Formel zu bestimmen, muss der Forscher natürlich eine Vorstellung von der räumlichen Struktur seiner Moleküle haben.
Wenn kein äußeres elektrisches Feld vorhanden ist, sind die Achsen der molekularen Dipole aufgrund der thermischen Bewegung willkürlich ausgerichtet, sodass auf der Oberfläche des Dielektrikums und in jedem Element seines Volumens die elektrische Ladung im Durchschnitt Null ist. Wenn jedoch ein Dielektrikum in ein äußeres Feld eingebracht wird, kommt es zu einer teilweisen Ausrichtung der molekularen Dipole. Dadurch entstehen unkompensierte makroskopisch verbundene Ladungen auf der Oberfläche des Dielektrikums, die ein zum äußeren Feld gerichtetes Feld erzeugen.
Beispiele für polare Dielektrika sind: chlorierte Kohlenwasserstoffe, Epoxid- und Phenol-Formaldehydharze, Silizium-Silizium-Verbindungen usw. Bemerkenswerte Beispiele für polare Moleküle sind beispielsweise auch Wasser- und Alkoholmoleküle. Polare Dielektrika werden häufig in verschiedenen Technologiebereichen eingesetzt, beispielsweise in der Piezoelektrizität und Ferroelektrizität, in der Optik, in der nichtlinearen Optik, in der Elektronik, in der Akustik usw.

