Batterien. Berechnungsbeispiele
 Batterien sind elektrochemische Stromquellen, die nach der Entladung mit elektrischem Strom aus einem Ladegerät aufgeladen werden können. Wenn der Ladestrom in der Batterie fließt, kommt es zur Elektrolyse, wodurch an Anode und Kathode chemische Verbindungen gebildet werden, die sich im anfänglichen Betriebszustand der Batterie an den Elektroden befanden.
Batterien sind elektrochemische Stromquellen, die nach der Entladung mit elektrischem Strom aus einem Ladegerät aufgeladen werden können. Wenn der Ladestrom in der Batterie fließt, kommt es zur Elektrolyse, wodurch an Anode und Kathode chemische Verbindungen gebildet werden, die sich im anfänglichen Betriebszustand der Batterie an den Elektroden befanden.
Elektrische Energie wird beim Laden in einer Batterie in eine chemische Energieform umgewandelt. Bei der Entladung wird die chemische Energieform in elektrische umgewandelt. Zum Laden einer Batterie wird mehr Energie benötigt, als durch Entladen gewonnen werden kann.
Die Spannung jeder Zelle eines Blei-Säure-Akkus sollte nach dem Laden 2,7 V betragen und beim Entladen nicht unter 1,83 V sinken.
Die durchschnittliche Spannung einer Nickel-Eisen-Batterie beträgt 1,1 V.
Die Lade- und Entladeströme der Batterie sind begrenzt und vom Hersteller festgelegt (ca. 1 A pro 1 dm2 der Platte).
Die Strommenge, die einer geladenen Batterie entnommen werden kann, wird als Amperestundenkapazität der Batterie bezeichnet.
Batterien zeichnen sich auch durch Energie- und Stromeffizienz aus.Die Energierückgabe entspricht dem Verhältnis der beim Entladen aufgenommenen Energie zur beim Laden der Batterie aufgewendeten Energie: ηen = Araz / Azar.
Für eine Blei-Säure-Batterie beträgt ηen = 70 % und für eine Eisen-Nickel-Batterie ηen = 50 %.
Die Stromabgabe ist gleich dem Verhältnis der beim Entladen aufgenommenen Strommenge zur beim Laden verbrauchten Strommenge: ηt = Q mal / Qchar.
Blei-Säure-Batterien haben ηt = 90 % und Eisen-Nickel-Batterien ηt = 70 %.
Batterieberechnung
1. Warum ist die Stromrückgabe der Batterie größer als die Energierückgabe?
ηen = Araz / Azar = (Up ∙ Ip ∙ tp) / (Uz ∙ Iz ∙ tz) = Up / Uz ∙ ηt.
Die Energierückgabe ist gleich der Stromrückgabe ηt multipliziert mit dem Verhältnis der Entladespannung zur Ladespannung. Da das Verhältnis Uр / U3 <1 ist, ist ηen <ηt.
2. In Abb. ist eine Blei-Säure-Batterie mit einer Spannung von 4 V und einer Kapazität von 14 Ah dargestellt. 1. Die Verbindung der Platten ist in Abb. dargestellt. 2. Die Parallelschaltung der Platten erhöht die Batteriekapazität. Um die Spannung zu erhöhen, werden zwei Plattensätze in Reihe geschaltet.
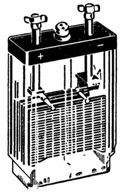
Reis. 1. Blei-Säure-Batterie
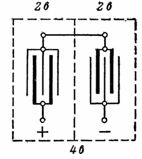
Reis. 2. Anschließen der Platten einer Blei-Säure-Batterie für eine Spannung von 4 V
Die Batterie wird in 10 Stunden mit einem Strom von Ic = 1,5 A geladen und in 20 Stunden mit einem Strom von Ip = 0,7 A entladen. Wie hoch ist die Stromeffizienz?
Qp = Ip ∙ tp = 0,7 ∙ 20 = 14 A • h; Qz = Iz ∙ tz = 1,5 ∙ 10 = 15 A • h; ηt = Qp / Qz = 14/15 = 0,933 = 93 %.
3. Der Akku wird 5 Stunden lang mit einem Strom von 0,7 A geladen. Wie lange entlädt es sich bei einem Strom von 0,3 A bei einer Stromabgabe von ηt = 0,9 (Abb. 3)?
Reis. 3. Abbildung und Diagramm für Beispiel 3
Die zum Laden der Batterie verbrauchte Strommenge beträgt: Qz = Iz ∙ tz = 0,7 ∙ 5 = 3,5 A • h.
Die während der Entladung freigesetzte Strommenge Qp wird nach der Formel ηt = Qp / Qz berechnet, wobei Qp = ηt ∙ Qz = 0,9 ∙ 3,5 = 3,15 A • h.
Entladezeit tp = Qp / Ip = 3,15 / 0,3 = 10,5 Stunden.
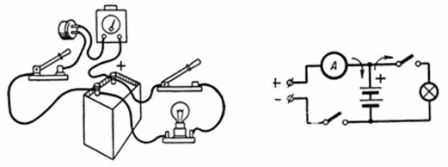
4. Die 20-Ah-Batterie wurde innerhalb von 10 Stunden am Wechselstromnetz über einen Selengleichrichter vollständig aufgeladen (Abb. 4). Der Pluspol des Gleichrichters wird beim Laden mit dem Pluspol der Batterie verbunden. Mit welchem Strom wird die Batterie geladen, wenn der Stromwirkungsgrad ηt = 90 % ist? Mit welchem Strom kann die Batterie innerhalb von 20 Stunden entladen werden?
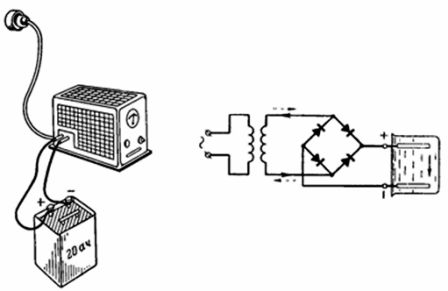
Reis. 4. Abbildung und Diagramm für Beispiel 4
Der Batterieladestrom beträgt: Ic = Q / (ηt ∙ tc) = 20 / (10 ∙ 0,9) = 2,22 A. Zulässiger Entladestrom Ið = Q / tr = 20/20 = 1 A.
5. Eine Akkumulatorbatterie bestehend aus 50 Zellen wird mit einem Strom von 5 A geladen. Eine Batteriezelle hat 2,1 V und ihr Innenwiderstand rvn = 0,005 Ohm. Wie hoch ist die Batteriespannung? Was ist usw. c. muss ein Ladungsgenerator mit Innenwiderstand rg = 0,1 Ohm vorhanden sein (Abb. 5)?
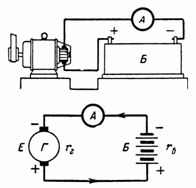
Reis. 5. Abbildung und Diagramm für Beispiel 5
Gleichstrombatterie ist gleich: Eb = 50 ∙ 2,1 = 105 V.
Innenwiderstand der Batterie rb = 50 ∙ 0,005 = 0,25 Ohm. D. d. S. Generator ist gleich der Summe von e. usw. mit Batterien und Spannungsabfall in Batterie und Generator: E = U + I ∙ rb + I ∙ rg = 105 + 5 ∙ 0,25 + 5 ∙ 0,1 = 106,65 V.
6. Der Akku besteht aus 40 Zellen mit Innenwiderstand rvn = 0,005 Ohm und z. usw. S. 2,1 V. Die Batterie wird mit dem Strom I = 5 A vom Generator geladen, z.B. usw. mitDas sind 120 V und der Innenwiderstand rg = 0,12 Ohm. Bestimmen Sie den Zusatzwiderstand rd, die Leistung des Generators, die Nutzleistung der Ladung, die Verlustleistung im Zusatzwiderstand rd und die Verlustleistung in der Batterie (Abb. 6).
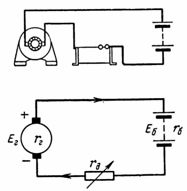
Reis. 6. Berechnung des Akkumulators
Finden Sie zusätzlichen Widerstand mit Kirchhoffs zweites Gesetz:
Eg = Eb + rd ∙ I + rg ∙ I + 40 ∙ rv ∙ I; rd = (Eg-Eb-I ∙ (rg + 40 ∙ rv)) / I = (120-84-5 ∙ (0,12 + 0,2)) / 5 = 34,4 / 5 = 6,88 Ohm …
Da e. usw. c. Wenn der Akku geladen ist, beträgt die EMF der Zelle zu Beginn des Ladevorgangs 1,83 V. Zu Beginn des Ladevorgangs beträgt der Strom bei konstantem Zusatzwiderstand mehr als 5 A. Um einen konstanten Ladevorgang aufrechtzuerhalten Stromstärke, ist es notwendig, den Zusatzwiderstand zu ändern.
Verlustleistung im Zusatzwiderstand ∆Pd = rd ∙ I ^ 2 = 6,88 ∙ 5 ^ 2 = 6,88 ∙ 25 = 172 W.
Verlustleistung im Generator ∆Pg = rg ∙ I ^ 2 = 0,12 ∙ 25 = 3 W.
Verlustleistung im Innenwiderstand der Batterie ∆Pb = 40 ∙ rvn ∙ I ^ 2 = 40 ∙ 0,005 ∙ 25 = 5 W.
Die vom Generator an den externen Stromkreis gelieferte Leistung beträgt Pg = Eb ∙ I + Pd + Pb = 84 ∙ 5 + 172 + 5 = 579 W.
Nutzladeleistung Ps = Eb ∙ I = 420 W.